中科院高福院士课题组 2019 年发表的重要的研究成果
高福,中国科学院微生物研讨所病原微生物与免疫学要点实验室主任、中国科学院院士、美国科学院外籍院士、中国疾病防备控制中心主任、国家自然科学基金委员会副主任。
首要研讨范畴:囊膜病毒与结构免疫学,要点关注以流感为代表的新发、再发流行症,研讨病毒宿主互作形式、跨种传达机制以及病毒特异性的 T 细胞免疫与分子辨认等。
近年来在 Cell, Nature, Science, The Lancet, PNAS 等尖端期刊宣布多篇论文。
2019 年高福院士一共宣布论文 59 篇,限于篇幅下面选取其间 12 篇高价值论文,来介绍一下高福院士与他的病毒斗士们的丰盛成果。
Cell:Human Neonatal Fc Receptor Is the Cellular Uncoating Receptor for Enterovirus B(人类新生儿 Fc 受体是肠病毒 B 的细胞脱壳受体)
肠病毒 B (EV-B) 归于小核糖核酸病毒科肠病毒属,是人类严峻流行症的病原体。
研讨人员发现人类新生儿的 Fc 受体 (FcRn) 是首要 EV-B 的脱壳受体。FcRn 经过其 FCGRT 亚基与「峡谷」(canyon) 中的病毒颗粒结合。
经过以原子或近原子分辨率在病毒进入的不同阶段取得多个冷冻电镜结构,破译了肠病毒附着和脱壳的潜在机制。
这些结构标明,与附着受体 CD55 不同,FcRn 与病毒粒子的结合在酸性条件下诱导「口袋因子」(pocket factor)有用开释,并引发病毒粒子构象的改动,为了解肠道病毒的进入机制供给了结构根底。
https://doi.org/ 10.1016 /j.cell.2019.04.035
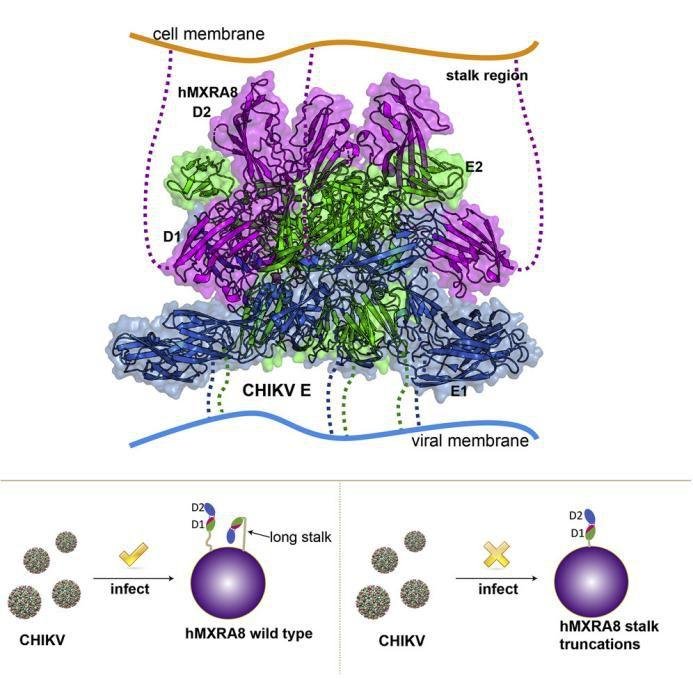
Cell:Molecular Basis of Arthritogenic Alphavirus Receptor MXRA8 Binding to Chikungunya Virus Envelope Protein(甲病毒受体 MXRA8 与基孔肯雅病毒包膜蛋白结合的分子根底)
虫源性甲病毒,如基孔肯雅病毒 (CHIKV),可在全世界范围内引起严峻和使人衰弱的风湿病,造成严峻的经济损失。之前的研讨发现 MXRA8 是病毒进入细胞的受体。
在这里,研讨人员 揭示了小鼠 MXRA8、人 MXRA8 与 CHIKV E 蛋白复合物的晶体结构,以及人 MXRA8 和 CHIKV 病毒样颗粒的冷冻电镜结构。
图片来历:Cell
MXRA8 具有两个共同拓扑结构的类 Ig 域。结合体之间的原子细节标明,MXRA8 的两个域和铰链区都参加了两个前体 CHIKV E1 -E2 残基的相互效果。
值得注意的是,MXRA8 的茎区对 CHIKV 病毒的进入至关重要。这一发现为开发针对这些虫源性甲病毒的医治对策供给了重要信息。
https://doi.org/ 10.1016 /j.cell.2019.04.008
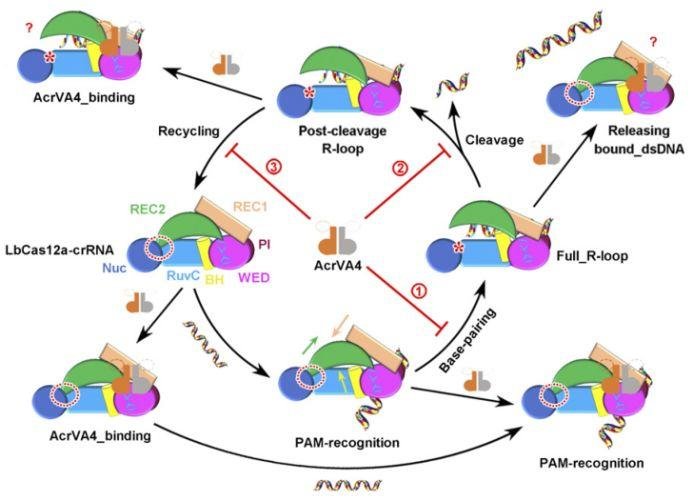
PNAS:Structural insight into multistage inhibition of CRISPR-Cas12a by AcrVA4(AcrVA4 对 CRISPR-Cas12a 多级按捺的结构研讨)
原核生物利有 CRISPR-Cas 系统来排除寄生捕食者,如噬菌体和移动遗传元件 (MGEs)。反过来,这些捕食者编码抗 CRISPR (Acr) 蛋白以逃避 CRISPR-Cas 免疫。
有研讨标明,一种按捺 CRISPR-Cas12a 系统的 Acr 蛋白——AcrVA4 被证明能够削减人纤毛杆菌科细菌 Cas12a(LbCas12a)介导的人类细胞基因组修改,但其潜在机制仍不清楚。
研讨人员 解析了 AcrVA4 与 crRNA 负载的 LbCas12a 结合的冷冻电镜结构,发现不同于其他只针对 1 个阶段的特征型 Acr 按捺剂,AcrVA4 能够在 CRISPR-Cas 作业通路的几个阶段按捺 LbCas12a。
这项研讨强调了 AcrVA4 的多功能性,并为开发调控基因组修改东西供给了头绪。
https://doi.org/ 10.1073 /pnas.1909400116
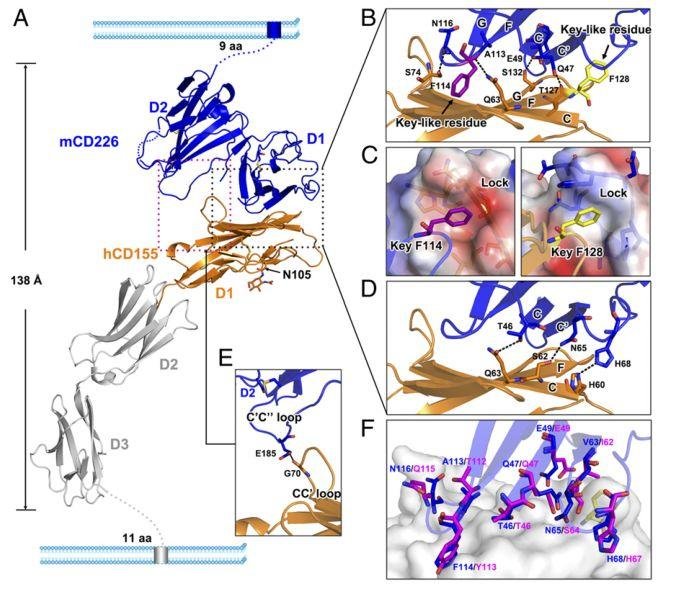
PNAS:Binding mode of the side-by-side two-IgV molecule CD226 /DNAM- 1 to its ligand CD155 /Necl- 5(并排的两个 IgV 分子 CD226 / DNAM- 1 与配体 CD155 / Necl- 5 的结合形式)
CD226 /DNAM- 1 是一种在 NK 细胞中表达的刺激分子,它经过与 NK 细胞的配体 CD155 结合来调节 NK 细胞的功能。
研讨人员 经过测定载脂蛋白 CD226 和 CD226 -CD155 复合物的结构,讨论激活受体 CD226 和 CD155 相互效果的分子根底。
CD226 显现了其两个免疫球蛋白 V-set (IgV) 域共同的并排形式,该形式与已知的 Ig-like 分子都基本不同。CD226 和 CD155 的结合谱标明,这两个 IgV 域都参加了配体结合。
图片来历:PNAS
该研讨在结构上支撑更好地了解 NK 细胞激活,有助于肿瘤免疫医治生物制剂的发展。
https://doi.org/ 10.1073 /pnas.1815716116
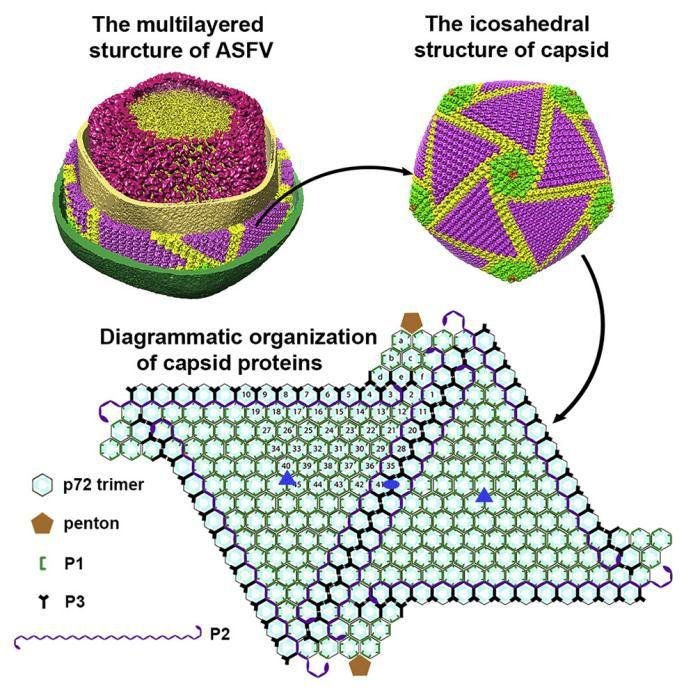
Cell Host & Microbe:Cryo-EM Structure of the African Swine Fever Virus(非洲猪瘟病毒的冷冻电镜结构)
非洲猪瘟病毒 (ASFV) 是具有二十面体多层结构的大型双链 DNA 病毒。ASFV 引起丧命的猪出血性疾病,现在已对亚洲猪肉业造成广泛损坏。
在这里,研讨人员 解析了 ASFV 的二十面体衣壳在 4.6 -Å 处的冷冻电镜 (Cryo-EM) 结构。
ASFV 颗粒由 8280 仿制的首要衣壳蛋白 p72、60 仿制的戊糖蛋白和至少 8340 个非必须衣壳蛋白组成,其间可能有 3 种不同类型。
非必须衣壳蛋白在外壳下方形成一个六边形网络,将相邻的衣壳蛋白「胶合」在一起,起到稳定剂的效果。
图片来历:Cell Host & Microbe
该发现供给了 ASFV 衣壳结构的全面分子模型,将有助于未来对策的发展,以及推进疫苗的研制。
https://doi.org/ 10.1016 /j.chom.2019.11.004
Nature Microbiology:Neutralization mechanism of human monoclonal antibodies against Rift Valley fever virus(人抗裂谷热单克隆抗体的中和机制)
裂谷热病毒 (RVFV) 是一种由蚊子传达的病原体,在家畜和人类中造成很多发病率和逝世率。迄今为止,还没有取得答应的人类疫苗或疗法。
研讨人员报告了针对 RVFV 包膜蛋白 Gn 和 Gc 的恢复患者单克隆抗体的别离。
与 Gc 特异性单克隆抗体相比,Gn 特异性单克隆抗体在体外表现出更高的中和活性,对小鼠 RVFV 感染的维护效果也更好。
Gn 单克隆抗体干扰可溶性 Gn 与细胞的结合,经过阻断病毒粒子与宿主细胞的结合来防备感染。
图片来历:Nature Microbiology
研讨结果强调了基于抗体的医治潜力,并为规划 RVFV 疫苗供给了基于结构的理论根底。
https://doi.org/ 10.1038 /s41564 – 019 – 0411 -z
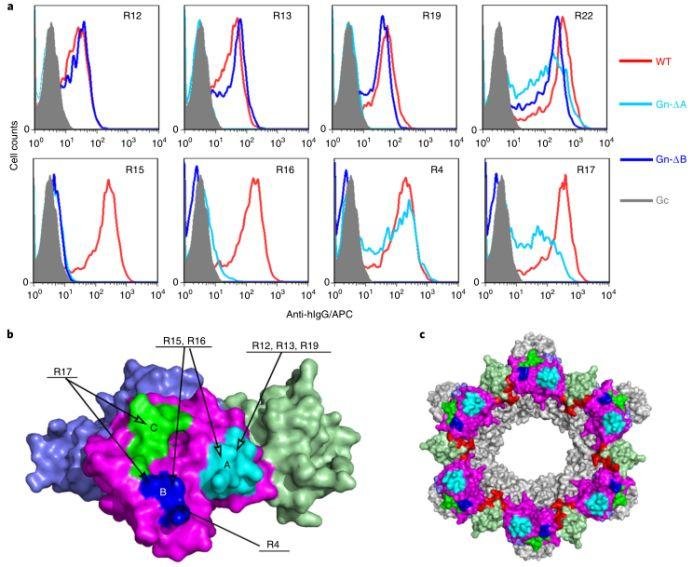
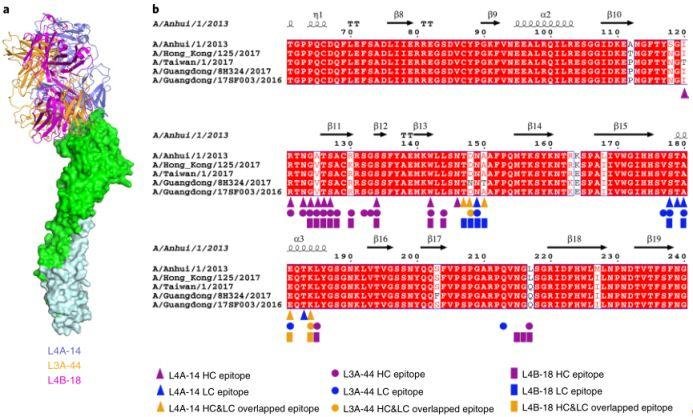
Nature Microbiology:Structure-function analysis of neutralizing antibodies to H7N9 influenza from naturally infected humans(人自然感染 H7N9 流感中和抗体的结构功能剖析)
人类自然感染 H7N9 病毒后发生的 H7 反应性抗体库的特异性和中和广度现在尚不清楚。
2013 年和 2014 年,研讨人员从 4 例感染的供体外周血 B 细胞中别离并判定了 73 个 H7 反应性单克隆抗体。
在这些抗体中,45 个是 H7 特异性的,其间 17 个中和了病毒。另外一组 28 个抗体,在结合实验中 H7 和 H3 血凝素发生交叉反应,并积累了很多的体细胞突变,但在体外首要是非中和的。
图片来历:Nature Microbiology
但是,在 2016 – 2017 年别离出的 17 种中和抗体中,只要 3 种对长江三角洲世系病毒保持活性,这些病毒现已发生了抗原变化,这就强调了更新 H7N9 疫苗的必要性。
https://www.nature.com/articles/s41564 – 018 – 0303 – 7
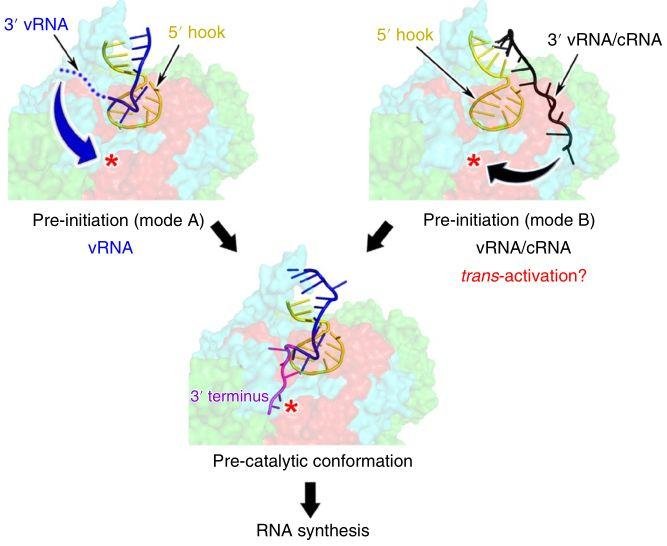
Nature Microbiology:Structural insight into RNA synthesis by influenza D polymerase(流感 D 聚合酶组成 RNA 的结构研讨)
流感病毒聚合酶运用加帽的 RNA 引物启动转录,并经过结合保守的病毒基因组 RNA (vRNA) 或互补 RNA (cRNA) 启动子,结合结尾和内部的启动子,进行两步仿制进程。
研讨人员运用冷冻电镜 解析了载脂蛋白和启动子结合的 D 型流感病毒聚合酶结构,发现该聚合酶具有进化保守的稳定中心结构和固有的柔性外周结构域。
功能研讨证真实 vRNA 启动子的两个构象 (形式 A、B) 中,B 型构象对中间 cRNA 组成 vRNA 的关键效果,但与 cRNA 发生无关,首要受 A 型构象调控。
图片来历:Nature Microbiology
该作业增进了对流感病毒聚合酶组成不同 RNA 物种的调控机制的了解,为抗病毒药物的规划拓荒了新的机会。
https://doi.org/ 10.1038 /s41564 – 019 – 0487 – 5
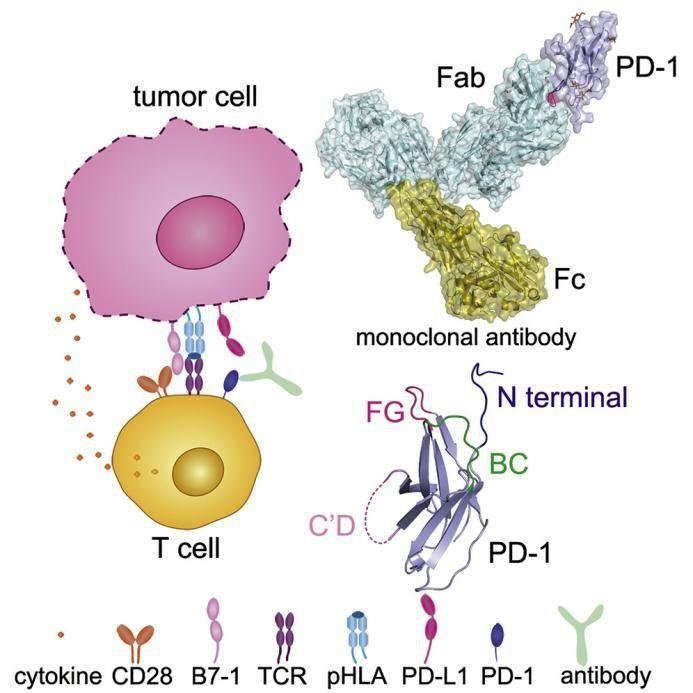
iscience:The FG Loop of PD- 1 Serves as a “Hotspot” for Therapeutic Monoclonal Antibodies in Tumor Immune Checkpoint Therapy(PD- 1 的 FG 环是肿瘤免疫检查点医治中单克隆抗体的「热门」)
PD- 1 /PD-L1 阻断单克隆抗体 (mAbs) 已成为肿瘤免疫检查点医治的中心。辨认 PD- 1 单克隆抗体的「热门」将有助于开发下一代长效口服给药制剂。
研讨人员判定了两种 PD- 1 靶向的单克隆抗体——GY- 5、GY- 14。这两种单克隆抗体首要结合 PD- 1 的 FG 环,与 PD-L1 存在多种相互效果。
FG 环与不同的单克隆抗体结合后,其构象发生了很大的变化。
PD- 1 的糖基化润饰能够在 4 个潜在的 N 端糖基化位点中的 3 个位点上观察到。但是,GY- 5 和 GY- 14 与 PD- 1 的结合不受糖基化的影响。
图片来历:iscience
这些发现拓宽了对立 PD- 1 单克隆抗体机制的了解,并为靶向 PD- 1 的药物的开发供给了思路。
https://doi.org/ 10.1016 /j.isci.2019.03.017
Plos Biology:Peptide presentation by bat MHC class I provides new insight into the antiviral immunity of bats(蝙蝠 MHC I 类多肽表达为蝙蝠抗病毒免疫供给了新的视角)
蝙蝠带有许多人畜共患病毒,包括人类和其他哺乳动物的高致病性病毒。
为了进一步了解蝙蝠的抗病毒免疫性,研讨人员挑选并判定了一系列蝙蝠首要组织相容性复合体(MHC)I Ptal-N * 01:01 - 结合肽,它们衍生自四种不同的蝙蝠传达病毒,即亨德拉病毒 (HeV)、埃博拉病毒(EBOV)、中东呼吸综合征冠状病毒(MERS-CoV) 和 H17N10 流感样病毒。
Ptal-N * 01:01 的结构显现出不寻常的肽呈递特征,在经典的首要锚固位置,Ptal-N * 01:01 的 B 和 F 也显现出非常规的构象,这导致异常的肽基序和不同的肽呈递。
图片来历:Plos Biology
研讨揭示了蝙蝠的适应性免疫,有助于对人类有害的蝙蝠传达病毒的疫苗开发。
https://doi.org/ 10.1371 /journal.pbio.3000436
Mbio:Crystal Structure of African Swine Fever Virus dUTPase Reveals a Potential Drug Target(非洲猪瘟病毒 dUTPase 的晶体结构揭示了潜在的药物靶标)
E165R 是非洲猪瘟病毒 (ASFV) 基因组编码的高度特异性 dUTP 核苷酸水解酶 (dUTPase),是在猪巨噬细胞中高效仿制 ASFV 所必需的。
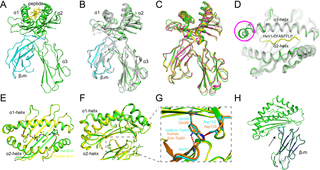
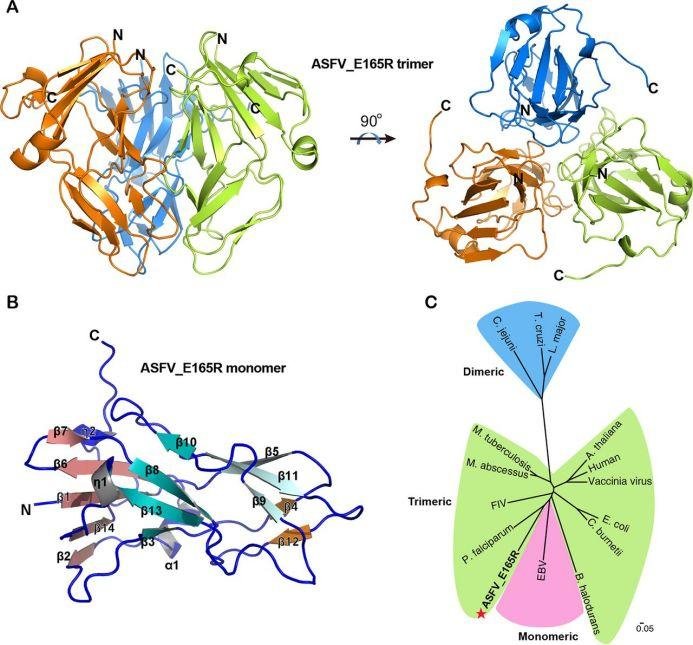
研讨人员解析了 E165R 处于脱脂状况且与其产物 dUMP 复杂的高分辨率晶体结构。明确了酶活性位点的结构,以及活性位点与转储配体之间的相互效果。
将 ASFV E165R 结构与其他物种的 dUTPase 结构进行比较,发现 E165R 的活性位点与结核分枝杆菌和恶性疟原虫的 dUTPases 活性位点高度类似,针对这种活性点开发小分子化学物质,可能是潜在的 ASFV 候选药物。
图片来历:Mbio
研讨结果为靶向 E165R 的抗 ASFV 药物规划供给了重要依据。
https://doi.org/10.1128 /mBio.02483 – 19
Cell Reports:Double Lock of a Human Neutralizing and Protective Monoclonal Antibody Targeting the Yellow Fever Virus Envelope(靶向黄热病病毒包膜的人中和维护性单克隆抗体的机制)
黄热病病毒 (YFV) 是一种丧命的人类病原体。YFV 在非洲和巴西重新呈现,导致数百人逝世,而且一些病例已输入中国,迫切需要防备和医治对策。
此前,研讨人员经过噬菌体展示技能挑选出了几种抗 YFV 单克隆抗体。
本研讨发现其间一个 5A 具有高中和效力和良好的维护效果。YFV 包膜蛋白交融前后的晶体学剖析标明,其构象与黄病毒其他 E 蛋白构象类似。
在两种状况下与 E 蛋白复合的 5A 结构得到解析,从而 揭示了一个不变的辨认位点。结构剖析和功能数据标明 5A 经过阻止病毒附着和交融来干扰病毒进入,具有很高的中和潜能。
图片来历:Cell Reports
https://doi.org/ 10.1016 /j.celrep.2018.12.065
正文完