昨日,学术界震动,著名科学家 饶毅教授一口气告发“三位大咖”学术不端 ,饶毅教授回复说: 这封信并没有发出去,是他写的一篇草稿。这个回复也证实了这封信内容确是出于饶毅教授。
无疑。
我一向很钦佩饶毅教师,很赏识他在科学界所做的一些事情,包括兴办《知识分子》和在转基因科普方面所做的尽力。在这封信的终究,他给基金委提了三点建议,实名告发了三位科研工作者涉嫌学术造假。我十分赏识饶毅的这种气魄,也十分支撑相关部门对告发的真实性进行核实,严惩造假者。本来我能够做一个旁观者,静观事态发展。但饶毅教师对上海生化细胞所裴钢教师造假的指控内容让人实在不能服气。


裴钢,1953 年 12 月 11 日出生于辽宁省沈阳市,细胞生物学家,中国科学院院士、发展中国家科学院院士,同济大学校长。1970 年裴钢参加工作。1978 年进入沈阳药科大学学习,先后取得学士、硕士学位;1991 年取得美国北卡罗莱纳州立大学博士学位;1992 年至 1995 年在美国杜克大学进行博士后研讨;1995 年 3 月回国,并担任中国科学院 / 德国马普学会青年科学家小组组长;1996 年获国家杰出青年科学基金;1999 年当选为中国科学院院士;2000 年至 2007 年担任中国科学院上海生命科学研讨院院长;2007 年 8 月起担任同济大学校长。裴 钢主要从事 细胞信号转导及其调控机理的研讨。
置疑一个人学术造假,首要讲究的是依据。比如图片造假,或许数据重复,又或许有确切试验依据证明数据无法重复等。那饶毅教师的依据是什么呢?“众所周知 GPCR 需求七重跨膜区域才有功用,裴钢声称只需 5 重跨膜,并且居然两个 GPCRs 都是这样的”。很难相信,这样的话居然出自饶毅之笔。
因为我不是研讨 GPCR 的,所以对其了解并不是许多。我知道 GPCR 有七重跨膜,但我不知道 GPCR 必须拥有全部的七重跨膜才有功用。所以饶毅教师的指控是树立在有大量试验依据证明 GPCR 只需缺了一个跨膜段就没有功用的基础之上。所以我就测验检索了一些文献,可惜因为时刻和能力有限,并没有找到一篇相关文献。真的期望有 GPCR 研讨相关范畴的同仁能给予指导。但不管怎样,目前饶毅教师也没有给出确凿依据,也没有任何人给出文献或试验数据支撑饶毅教师的说法。毕竟许多巨大的发现都违反从前的“众所周知”。已然这样,不如我们先来看看裴钢教师的这篇文章讲了什么。

在此之前,我先大体介绍一下 GPCR 的结构。G 蛋白偶联受体是一种七次跨膜蛋白受体,其 C 结尾和连接第 5 和第 6 个跨膜螺旋的胞内区都有 G 蛋白的结合位点。当胞外配体与 GPCR 结合后会引起 GPCR 构象改动,然后使得 G 蛋白与 GPCR 胞内区结合引起下游信号。
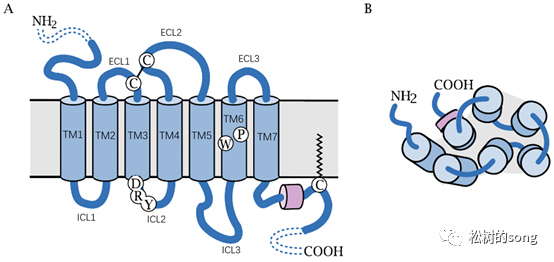
GPCRs 是一个十分大的家族,有近千种 GPCRs 基因,在多种生命过程中发挥重要作用。裴钢教师的研讨工作主要重视了 CCR5 和 CXCR4 这两种趋化因子受体。他们在克隆 CCR5 的时候意外得到一个缺失一段的基因,缺失的部分包括 TM1、ICL1、TM2 和 ECL1,终究得到了 5 次跨膜的部分缺失的 CCR5(mCCR5)。当他们把全长和 mCCR5 转入不表达 CCR5 的 HEK293 细胞中,发现全长和 mCCR5 都能够结合配体 RANTES 并产生趋化功用。别的 CXCR4 进行相同的删去骤变后也能够结合配体 SDF-1a 并产生趋化功用。所以文章最客观的定论应该是 CCR5 和 CXCR4 缺失 TM1、ICL1、TM2 和 ECL1 后依然能够结合相应配体 RANTES 或 SDF-1a 并发挥功用。那么如何来证明这个定论是否正确呢?最直接的便是重复试验。文章中的试验实际上十分简略,很简略重复。一重复就知道定论是否正确。假如得到相同的定论,造假之说不攻自破。假如重复不出来,那么再去评论是片面作假仍是试验设计漏洞。
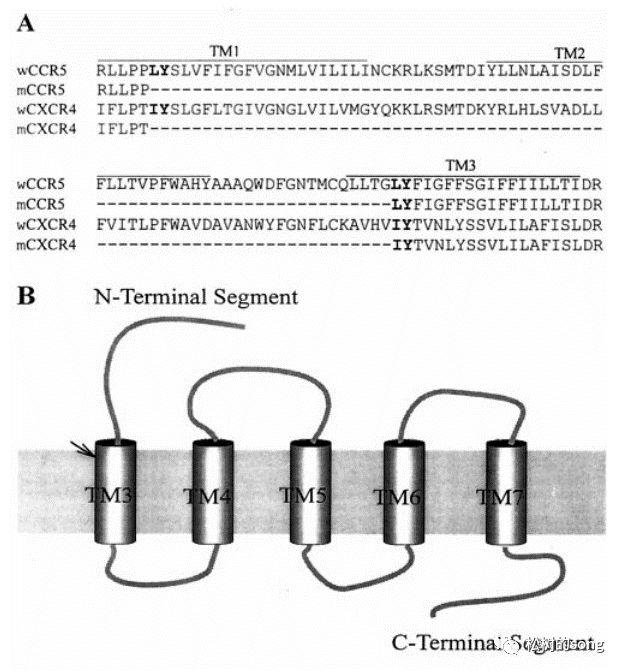
在没有直接试验数据的前提下,我们是否能够先依据已有的文献去推演一下缺失了 TM1、ICL1、TM2 和 ECL1 的 GPCR 是否有或许能够在特定配体的结合下发挥功用。所以我就检索了一些相关文献,和我们共享。得益于结构生物学的发展,CCR5 和 CXCR4 和配体结合的晶体结构已经被解析出来。因为我对结构生物学的剖析东西不是很在行,所以就没有详细剖析原始结构,我们能够依据文章中给出的图做一些简略的剖析。
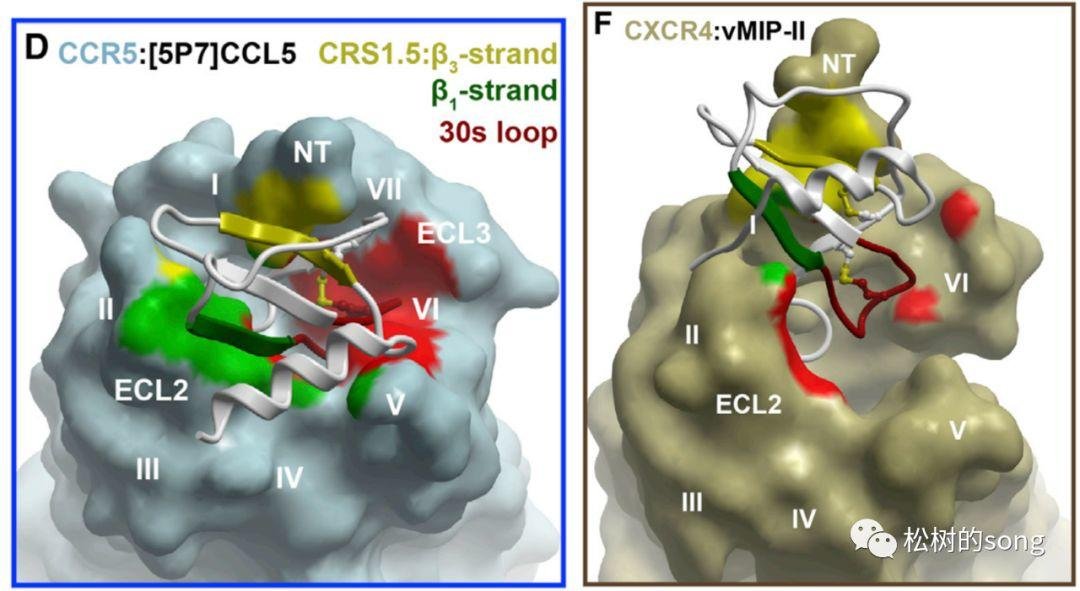
从结构来看 CCL5 (即 RANTES)的 b1-strand 和 CCR5 的 ECL2 (绿色)相互作用,CCL5 的 30s-loop 与 CCR5 的 ECL3 和深处的 5 - 7 跨膜段(赤色)相互作用,一起 CCL5 也与 N 端区域相互作用。我们能够看到 TM1、ECL1 和 TM2 与配体并没有显着的相互作用。CXCR4 与 vMIP-II 的相互作用也没有显着依靠 TM1、ECL1 和 TM2。所以,当删去 TM1、ICL1、TM2 和 ECL1 后,是有或许不影响 CCR5 和 CXCR4 与配体结合的。
已然删去上述部分是有或许不影响 GPCRs 与特定配体结合,那么会不会影响配体结合后的设想改变呢?对设想改变的研讨比较难,这儿就不得不说到范畴大牛 Brian K. Kobilka(2012 年诺贝尔化学奖)的一篇精彩的文章啦。
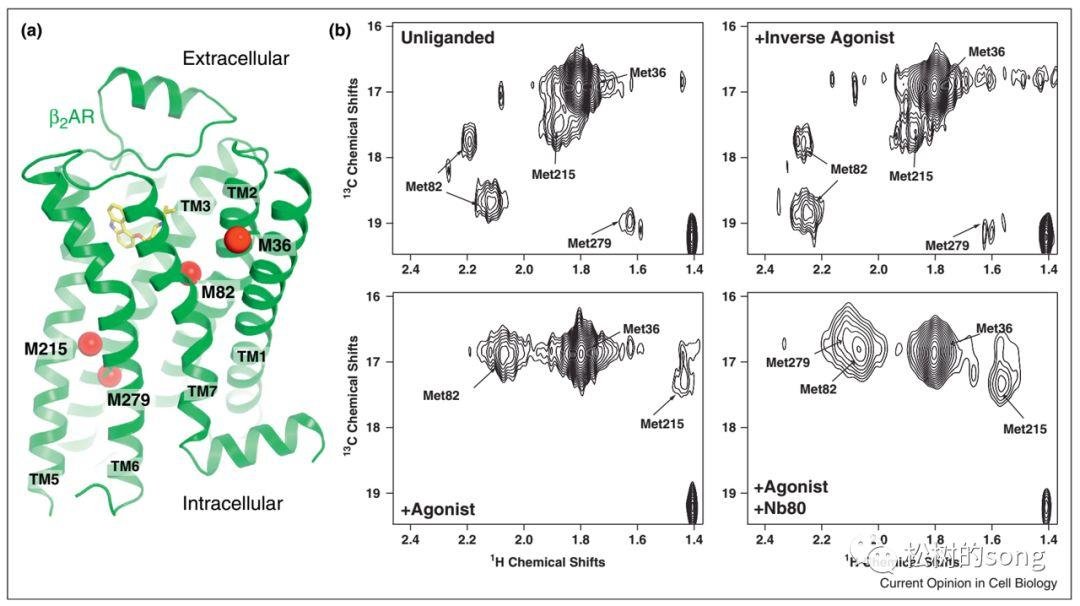
b2AR 是一种 GPCR,在结合配体后 TM2 中的 M82 有显着的化学位移改变,而 TM1 中的 M36 无显着改变。TM5 中的 M215 和 TM6 中 M279 在结合配体后也有显着的化学位移改变,说明配体结合导致了 TM5 和 TM6 的构象改变。在这个 GPCR 中 TM2 显着参加了配体结合,而 TM1 或许在配体结合和构象改变过程中的作用不显着。
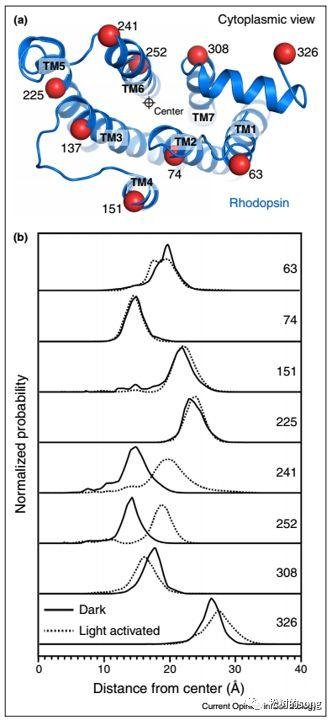
别的一项基于 double electron-electron resonance(DEER) spectroscopy 研讨发现,GPCR rhodopsin 的 TM1、TM2、TM7 在激活后没有显着的构象改变。
所以说,GPCRs 作为一我们族,不同的 GPCR 功用对不同区域的依靠是有很大差异的。更别说同一个 GPCR 能够结合不同配体产生不同的反应了,对不同区域的需求对于不同配体也不尽相同。从 GPCR 的视点来讲,整个信号无非便是配体结合导致构象改变,引起包内段与 G 蛋白结合。缺掉一部分或许这一切也能产生。那进化上为什么 CCR5 和 CXCR4 是 7 次跨膜而不是 5 次呢?这或许仅仅进化的前史原因,存在并不一定必须有用;又或许在配体区分过程中发挥作用(纯属猜想,欢迎吐槽)。
所以说,删掉 TM1、ICL1、TM2 和 ECL1 的 CCR5 和 CXCR4 能否发挥功用呢?我觉得不是“众所周知”的不或许。在 1999 年,或许这是个研讨 GPCRs 的一个不错的测验。至于定论是否正确,还待更有力的依据摆出。
参考资料
1. Kun Ling et. al., PNAS, 1999
2. watcut.uwaterloo.ca/webnotes/Pharmacology/GPCRs.html
3. Yi Zheng et. al., Immunity, 2017
4. Aashish Manglik and BrainKobilka, Current Opinion in Cell Biology, 2014
5. Rie Nygaard et. al., Cell, 2013
PS: 因为自己能力有限,如有过错欢迎纠正。作者并不站队,也十分敬仰两位前辈。仅仅期望我们能回归理性,尊重科学。