从人工智能到多功能干细胞诱导新技能,本年出现了一系列极具价值的新式技能,令人耳目一新。《The Scientist》梳理了 2019 年度具有代表性和突破性的生物技能。
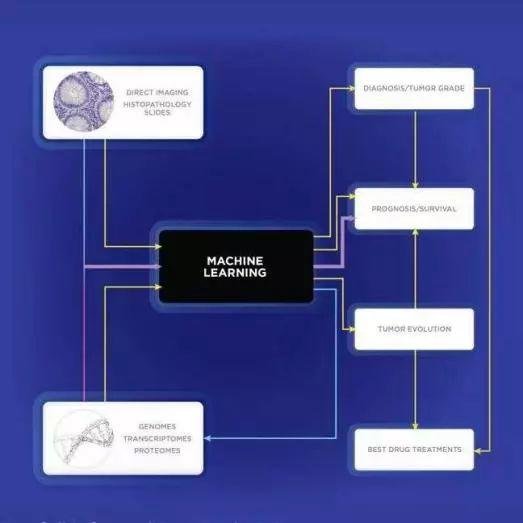
纵观本年生物学的许多重大发现,机器学习作为一种东西不断促进生命科学领域的发展。本年的很多研讨项目中,有研讨人员报导他们已成功经过机器学习来检查机体是否存在癌症或病原体感染;也有研讨人员经过机器学习鉴定血液样本中与糖尿病患者血管并发症相关的表观遗传标志物……
本年 8 月,麻省理工学院的研讨人员报导了使用 DNA 以及相似 CRISPR 的碱基修改机制记载细胞内部的生命活动,然后经过测序对其进行解码的办法。他们对大肠杆菌和人类细胞进行了工程改造,使它们能够记载多种分子事情以及它们发生的时间和次序。该办法的根本操作单位是两种类型的基因序列:一种在诱导型启动子的操控下编码特定的 gRNA,一种编码与核酸酶的 CRISPR-Cas9 酶 (与 gRNA 结合) 交融的碱基修改酶。遗传序列被转染到细胞中,当这些细胞露出于诱导剂 (诱导剂是试验人员希望在 DNA 中蚀刻的任何分子事情) 时,表达 gRNA 序列,RNA 结合到 Cas9-base 修改器交融蛋白,然后将其转运到方针 DNA 序列 (与 gRNA 匹配) 进行修改。这些修改能够稍后经过 DNA 测序进行分析。文章的共同作者,麻省理工学院的 Timothy Lu 说,这项研讨在环境毒素的检测和发育进程的记载方面也具有潜在的使用价值。【1】

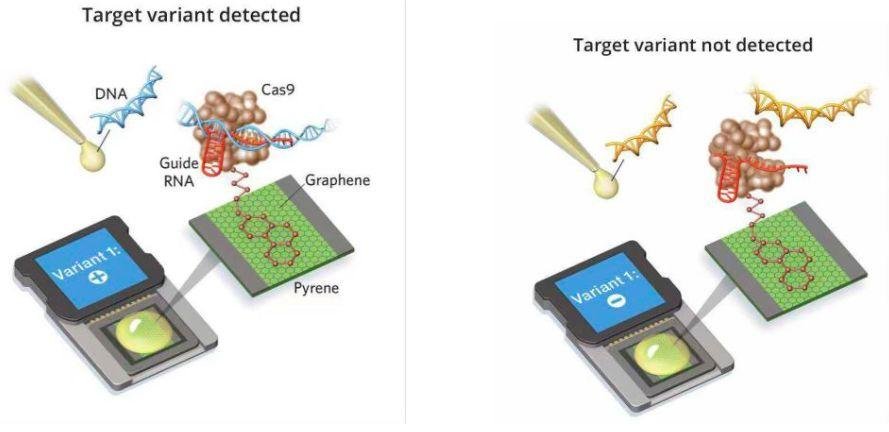
本年,根据 CRISPR-Cas9 修改进行的另一项创造性技能是开发了针对特定 DNA 序列的检测设备。现在,在很多试验室中主要采用方针扩增的方式,在 DNA 样本中寻觅特定的碱基序列。但这种办法需要耗费时间,还有或许产生偏差。为了防止方针扩增的缺点,加利福尼亚州Keck Graduate 研讨院Kiana Arand 的团队将研讨对象转向了 CRISPR-Cas 核酸酶家族,当它与特定的辅导 RNA 配对时,能够搜索整个基因组以发现并切开准确的序列。他们将 Cas9 酶与 RNA 和石墨烯芯片结合,且经过改造规划后不会切开 DNA。当 RNA-Cas9 复合物与其方针 DNA 序列连接,芯片内的电场就会发生变化,继而可进行阳性读数。
David Liu 及其团队研讨的修改技能 prime editing, 旨在经过防止双链 DNA 断裂来下降 CRISPR 的脱靶效应并提高 CRISPR 的准确性,该技能在本年 10 月于 Nature 宣告。PE 修改技能仅经过切开一条 DNA 单链增加、去除或取代碱基对,即可改写 DNA。它使用的是 CRISPR 体系中常用的 Cas9 核酸酶,但将该酶与一种名为 pegRNA 的引导 RNA 和别的一种逆转录酶相结合,后者能够向基因组中增加新的序列或碱基。一旦新的遗传物质掺入到 DNA 的切开链中,PE 就会对未修改的 DNA 链进行刻迹,向细胞发出信号对它进行重建, 并与已修改的链进行匹配【2】。
Shinya Yamanaka 在 2006 年初次宣告了诱导多功能干细胞的办法,该办法经过在分解过的细胞中过表达 Oct4,Sox2,Klf4,cMyc 四种转录因子,将细胞重置为多能状态,形成诱导多能干细胞(iPSC)。且 Oct4 是四个过表达的转录因子中最重要的一个。但在本年十一月,马克斯·普朗克分子生物医学研讨所 (Max Planck Institute for Molecular Biomedicine) 的 Sergiy Velychko 团队宣告,他们不只能在不调整 Oct4 水平的情况下制造出小鼠 iPSC,而且具有更高的功率。Yamanaka 在给《The Scientist》的邮件中谈道:“若这种新的办法可使用于人的细胞,将极有利于 iPS 细胞在临床上的使用。”【3】

[1] F.Farzadfard et al.,“Single-nucleotide-resolution computing and memory in living cells,”Molecular Cell ,75:P769-780.E4,2019.
[2]A.Anzalone et al.,“Search-and-replace genome editing without double-strand breaks or donor DNA,”Nature,doi:10.1038/s41586-019-1711-4,2019
[3]S. Velychko et al.,“Excluding Oct4 from Yamanaka cocktail unleashes the developmental potential of iPSCs,”Cell Stem Cell, doi:10.1016/j.stem.2019.10.002, 2019.