01
Nature Communications
2020 年 11 月 25 日,Nature Communications期刊(DOI:10.1038/s41467-020-19767-w)在线宣布浙江大学的标题为“Parabrachial nucleus circuit governs neuropathic pain-like behavior”的文章。浙江大学脑科学和脑医学学院讲师 孙丽 为论文榜首作者,研讨生 刘瑞 为一起榜首作者。孙丽和段树民 为一起通讯作者。
课题组研讨人员使用神经病理性痛苦模型(CPN)小鼠,结合在体神经元钙信号检测、电生理、光遗传学及行为学检测等,发现在给与神经病理性痛小鼠触觉和热刺激时,LPBN 谷氨酸(兴奋性)能神经元活动比对照小鼠明显增强,但 GABA(按捺性)能神经元活动无明显改变。用光遗传学选择性激活 LPBN 谷氨酸神经元则在正常小鼠也发生神经病理性痛的行为反响,而光遗传学按捺 LPBN 谷氨酸能神经元则对急性的生理性痛苦和缓慢的神经病理性痛苦都能阻断。有意思的是,光遗传学激活 GABA 能神经元(只占整体 LPBN 神经元的 10%)选择性按捺神经病理性痛,但不影响生理性痛苦。而按捺了 LPBN 的 GABA 能神经元则在正常小鼠也发生神经病理性痛苦样反响。
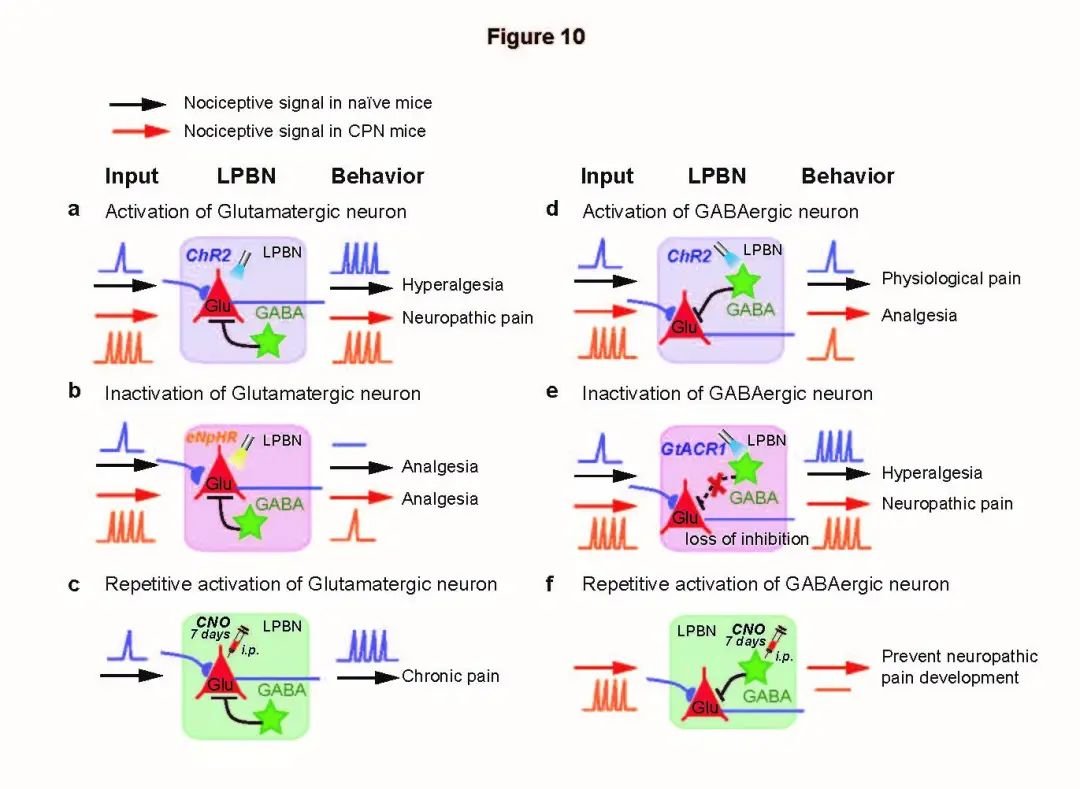
图 1 图文摘要:LPBN 环路调控生理性和病理性痛苦机制模式图
02

03
Nature Communications
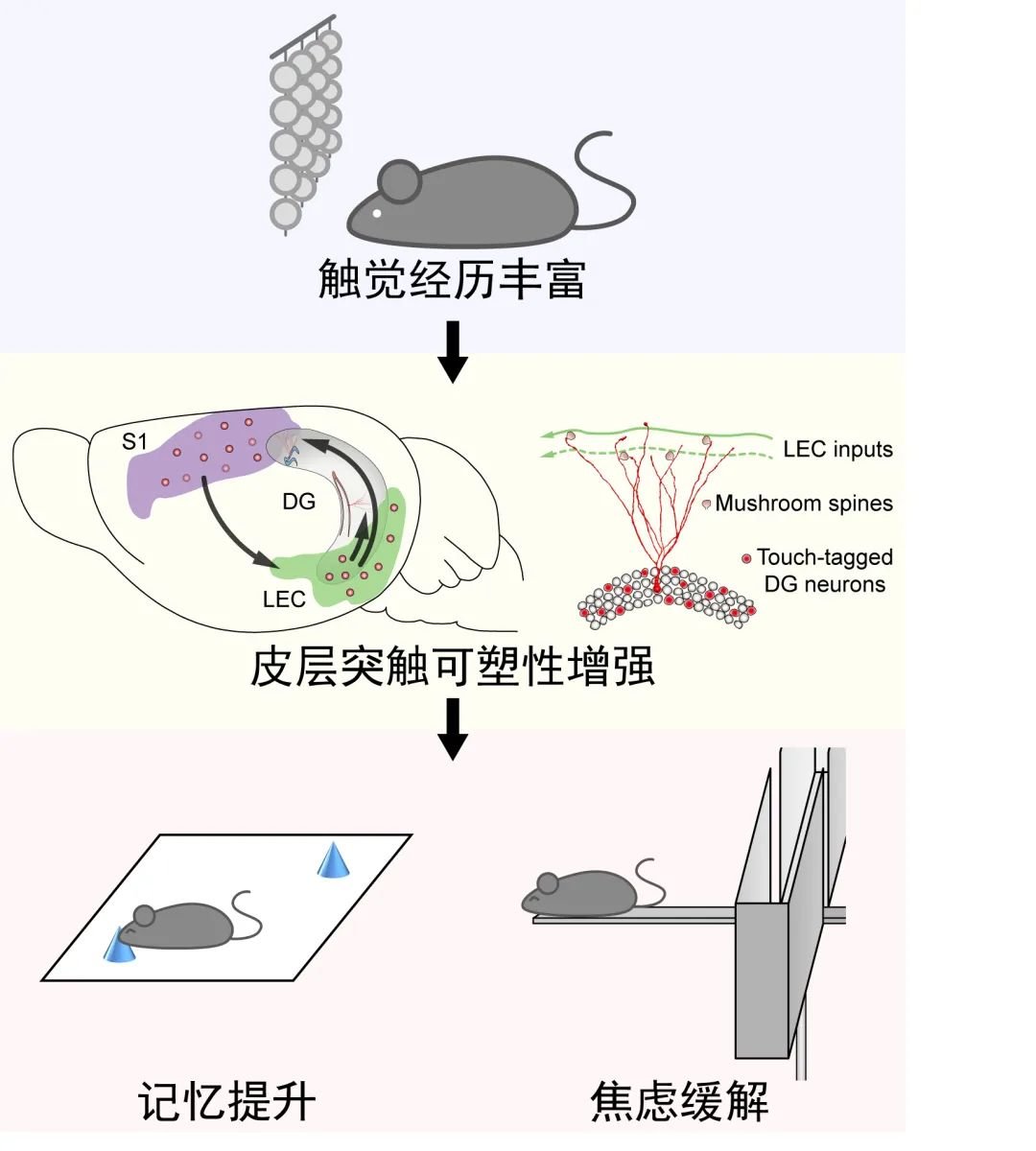
近日,浙江大学医学院 王晓东团队 采用簇新的单模态触觉丰厚和早年应激小鼠模型,结合行为学、活动神经元符号、化学遗传学、神经环路示踪和深度学习等技能,提醒了触觉丰厚促进回忆、缓解焦虑的神经环路机制。该研讨结果于 2020 年 11 月 27 日宣布于 Nature Communications 杂志(DOI: 10.1038/s41467-020-19874-8)。
首先,课题组经过在小鼠养殖笼内悬挂玻璃珠帘的方法,使小鼠在自在活动状态下频繁触摸温和的触觉刺激。继续的触觉阅历丰厚可明显提高小鼠在空间物体识别测试和高架十字迷宫测试中的行为表现,标明触觉丰厚具有促进空间回忆、缓解焦虑样行为的作用。
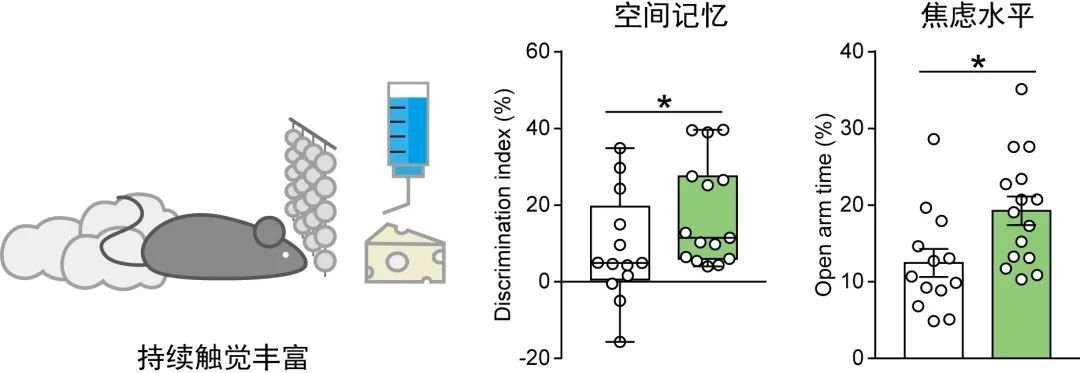
浙江大学脑科学和脑医学学院研讨生王驰、刘晖和李琨为论文一起榜首作者,王晓东研讨员为通讯作者。研讨得到了浙江大学段树民院士、汪浩教授、谷岩研讨员以及上海科技大学胡霁教授、南昌大学潘秉兴教授、德国马克斯·普朗克精神病学研讨所 Mathias Schmidt 博士等专家的大力支持,课题由科技部国家重点研制计划、国家自然科学基金资助。
04
Neuron
下丘脑存在着一群特殊的神经内分泌细胞,它们既保留了神经元的放电特性,又能够开释激素入血,作用于外周的靶器官,在调理机体生长发育、代谢生殖和内环境稳态中发挥着重要作用。其中,分泌血管加压素(AVP,又称抗利尿激素,ADH)和催产素(OXT)的神经元首要位于下丘脑室旁核(PVN)与视上核(SON),它们胞体大,轴突长且直接投射至神经垂体,构成下丘脑 - 神经垂体系统(Hypothalamo-Neurohypophysial System, HNS),即大细胞性神经内分泌系统(Magnocellular Neuroendocrine System, MNS)。从神经垂体开释入血的 AVP 与 OXT 调控机体的水盐平衡、临产与泌乳等重要过程,近年来药理学研讨显示 AVP 和 OXT 作为神经肽类神经调质,在脑内能调控机体的交际、恐惧和情感等,但内源性 OXT 是经过开释至外周后重新入脑,仍是大细胞内分泌神经元(MNCs)直接在脑内开释 OXT 发挥作用现在并不清楚。阐明内源性 OXT 的作用及机制依赖于对 MNCs 全脑投射的精密三维重构及其功用活动的精准靶向控制。
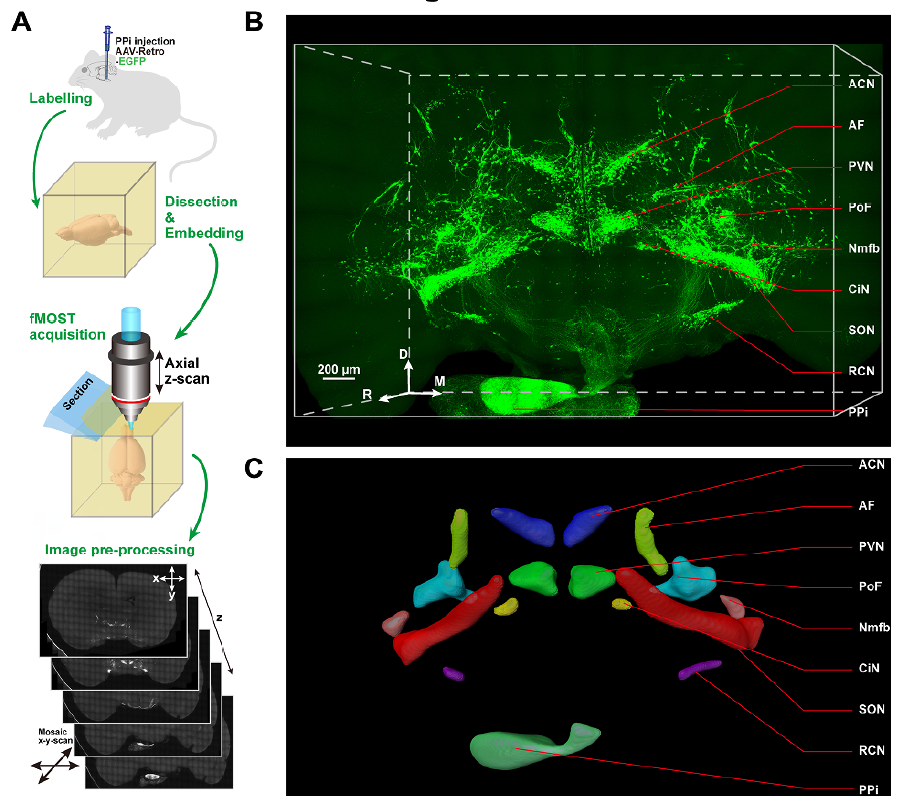
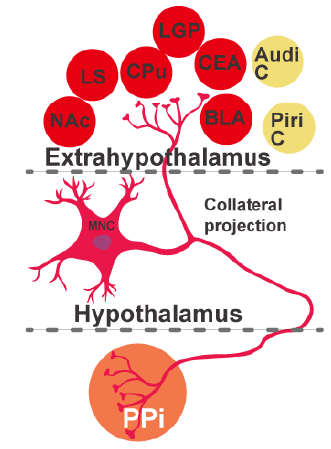
带着这些问题,浙江大学脑科学与脑医学学院 段树民院士 和高志华教授 的团队巧妙地将逆向示踪病毒打针至大鼠的神经垂体,使用病毒沿轴突高效逆向转运的特性,点亮整个 HNS。团队继而与华中科技大学武汉光电国家研讨中心 龚辉教授 团队协作,使用自主开发的 荧光显微光学切片断层成像(fMOST)技能,对大鼠全脑进行成像并初次完成了 HNS 高分辨率的三维重构(图 1)。研讨发现除了经典的 PVN 与 SON 外,下丘脑内多个核团都存在向神经垂体投射的 AVP 和 OXT 神经元,且部分 OXT 阳性大细胞能宣布轴突侧枝(collaterals)投射至皮层、杏仁核、伏隔核、纹状体等下丘脑外的区域,提示他们可能同时向外周和中枢内开释 OXT(图 1)。
为进一步探究 OXT 大细胞的功用,研讨人员构建了 OXT-Cre 转基因大鼠(在 OXT 阳性细胞中表达 Cre 重组酶),并在其神经垂体打针了 Cre 依赖、逆向转运的化学遗传学病毒,使用药物诱导,特异性控制 OXT 大细胞。研讨发现激活 OXT 大细胞不仅能经过投射至神经垂体的主轴突开释 OXT,提高外周血液中 OXT 的含量,也能经过脑内的侧枝开释 OXT,促进大鼠的交际行为;而按捺这些细胞则发生了相反的作用。提示 OXT 大细胞能在外周和中枢开释 OXT,协调机体稳态和中枢行为(图 3)。上述研讨结果于 2020 年 11 月 19 日 在线宣布于 Neuron 杂志(https://doi.org/10.1016/j.neuron.2020.10.032)。
05
Nature Communications
2020 年 11 月 12 日,Nature communications 在线宣布了浙江大学医学院 / 良渚实验室 夏宏光 团队的最新研讨成果:Pharmacological targeting of MCL-1 promotes mitophagy and improves disease pathologies in an Alzheimer’s disease mouse model。该研讨发现,MCL- 1 蛋白的特异性按捺剂 UMI-77 能够在模型小鼠中明显缓解阿尔兹海默症的病理特征,促进小鼠认知改善;初次提醒了 MCL- 1 作为线粒体自噬受体蛋白介导线粒体自噬的新机制;提出靶向 MCL- 1 蛋白诱导线粒体自噬是一种有巨大前景的医治阿尔兹海默症的策略。

该研讨发现,MCL- 1 是一种新的线粒体自噬受体蛋白;UMI-77 能够经过开释游离的 MCL- 1 蛋白诱导线粒体自噬,并逆转阿尔兹海默症的病理学特征。该研讨提示,MCL- 1 是一个医治阿尔兹海默症的新药物靶点;诱导线粒体自噬是医治阿尔兹海默症的有用策略。

浙江大学医学院、良渚实验室博士后 岑旭峰 , 徐晓燕 , 吴荣海 ,博士生 陈艳英 及台州学院讲师 何福生 为该论文的一起榜首作者。浙江大学医学院、良渚实验室 夏宏光 研讨员为首要通讯作者,哈佛大学 Ayaz Najafov 博士和台州学院 吴劼 教授为一起通讯作者。